CAR-T(카티)항암 관련주 : 박셀바이오, 앱클론, 유틸렉스
박셀바이오
항암면역치료제 연구개발업체. 주요 파이프라인은 Vax-NK 자연살해세포 항암면역치료제 플랫폼(간세포암)과 Vax-DC 수지상세포 항암면역치료제 플랫폼(다발골수종), Vax-CAR 시리즈 차세대 첨단 항암면역치료제 플랫폼으로 구성되어 있으며, 반려견 전용 항암면역치료제로 사이토카인 기반의 박스루킨-15 제품 보유.

앱클론
항체신약개발, 제조 및 판매업체. 난치성 암 또는 자가면역 질환 극복을 위한 바이오시너지 항체의약품(Biosynergy Antibody Therapeutics) 신약개발을 주요 사업으로 영위. CAR-T 치료제 등 면역치료제 개발에 신규로 진출. NEST(Novel Epitope Screening Technology) 플랫폼과 AffiMab(Affibody®-based bi-specific Antibody) 플랫폼 기술 보유. 주력제품으로는 위암 및 유방암 관련 AC101 항체치료제, 류마티스 관절염 관련 AM201(TNFa x IL-6) 이중항체치료제 등이 있음.

유틸렉스
면역항암 세포치료제와 면역항암 항체치료제 사업 등을 영위하는 업체. 차세대 면역 기반 항암제인 T 세포 치료제(EBViNT, WTiNT, TERTiNT, NYESOiNT), 항체치료제(EU101, EU102, EU103), CAR T 세포 치료제(MVR CAR-T, GPC3 CAR-T) 등을 개발 중.
https://www.cancer.gov/about-cancer/treatment/research/car-t-cells
CAR T 세포 : 환자의 면역 세포를 치료하여 암을 치료합니다.
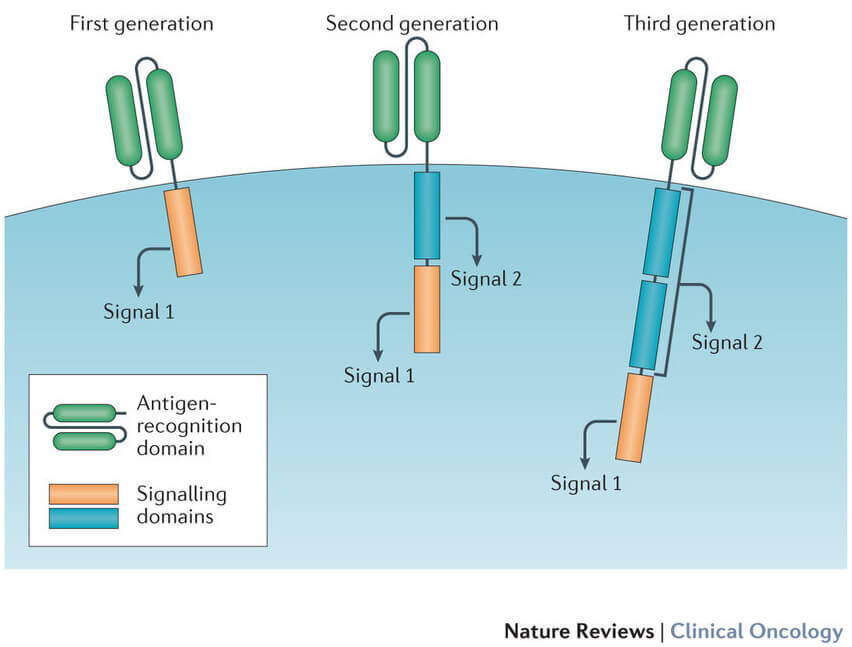
공동자극 신호전달 도메인은 주입 후 더 많은 T 세포를 생산하고 순환에서 더 오래 생존하는 그들의 능력을 향상시키기 위해 CAR T 세포의 새로운 세대에 추가되었다.
수십 년 동안 암 치료의 기초는 수술, 화학 요법 및 방사선 요법이었습니다. 이것들은 계속해서 치료의 중요한 주류가 되고 있지만, 새로운 범주의 치료는 최근 암 환자의 치료 그림을 변화시키는 데 도움이 되었습니다.
2000년대에는 이마티닙(Gleevec)과 트라스투주맙(허셉틴)과 같은 표적 치료법이 등장했는데, 이 치료법은 주로 이들 세포에서 나타나는 특정 분자 변화에 대해 호밍하여 암세포를 발견하고 죽이는 약물이다. 수십 가지 표적 치료법이 현재 많은 암에 대한 표준 치료법입니다.
그리고 지난 수십 년 동안 면역 요법 - 종양을 공격하기 위해 환자의 면역 체계의 힘을 입대시키고 강화시키는 치료법 -은 많은 사람들이 암 치료의 "다섯 번째 기둥"이라고 부르는 것이 급속히 자리 잡았습니다. 면역 체계를 향상시키는 약물이 진행성 암을 앓고있는 일부 사람들의 종양을 축소하고 심지어 근절하는 능력을 보여 주었기 때문입니다. 소수의 환자에서 이러한 치료 반응은 수년간 지속될 수 있습니다.
예를 들어, 면역 체크포인트 억제제라고 불리는 약물은 이미 흑색종, 폐, 신장, 방광 및 림프종을 포함한 많은 유형의 암을 가진 사람들을 치료하는 데 광범위하게 사용되고 있습니다.
그러나 CAR T-세포 요법이라고 불리는 또 다른 형태의 면역 요법은 연구자와 종양 전문의들 사이에서 상당한 흥분을 불러 일으켰습니다. CAR T 세포 치료법은 면역 체크포인트 억제제만큼 널리 사용되지는 않지만, 매우 진행된 백혈병과 림프종을 근절하고 수년 동안 암을 막는 동일한 능력을 보여주었습니다.면책 조항 종료.
2017년부터 여섯 개의 CAR T-세포 치료제가 FDA(Food and Drug Administration)의 승인을 받았습니다. 모두 림프종, 백혈병의 일부 형태, 그리고 가장 최근에는 다발성 골수종을 포함한 혈액 암의 치료를 위해 승인되었습니다.
이러한 치료법에 대한 흥분에도 불구하고, 그들은 더 적은 수의 장기 생존으로 이어집니다.면책 조항 종료 치료 된 환자의 절반 이상. 그들은 또한 가장 최근에 승인 된 CAR T 세포 요법의 경우 $ 450,000 이상인 비용에 대한 비판을 받았습니다.
그럼에도 불구하고, 수년간의 근면 연구 끝에 CAR T 세포 치료법은 암 치료의 주류에 진입했다고 면역 요법 및 CAR T 세포 요법의 선구자 인 NCI의 암 연구 센터 (CCR)의 외과 지부장 인 Steven Rosenberg 박사는 말했다.
"[CAR T 세포]는 현재 미국과 다른 국가에서 널리 이용 가능하며 공격적인 림프종 환자를위한 표준 치료법이되었습니다."라고 Rosenberg 박사는 말합니다. "그들은 현대 의학의 일부가되었습니다."

CAR T 세포 요법 : "살아있는 약물"
CAR T 세포는 "환자에게 살아있는 약물을 투여하는 것"과 동등하다고 CAR T 세포 분야의 또 다른 초기 리더 인 뉴욕의 Memorial Sloan Kettering Cancer Center의 Renier J. Brentjens, M.D., Ph.D.는 설명했다.
그들의 이름에서 알 수 있듯이, 면역 반응을 조율하고 병원균에 감염된 세포를 직접 죽이는 데 도움이되는 T 세포는 CAR T 세포 치료의 중추입니다.
현재 이용가능한 CAR T-세포 요법은 각각의 개별 환자에 대해 맞춤화된다. 그들은 환자로부터 T 세포를 수집하고 실험실에서 재 설계하여 키메라 항원 수용체 또는 CAR이라고 불리는 표면에 단백질을 생산함으로써 만들어집니다. CAR은 암세포 표면의 특정 단백질 또는 항원을 인식하고 결합합니다.

이 수용체는 "합성 분자, 그들은 자연적으로 존재하지 않는다"고 펜실베니아 대학 에이브람슨 암 센터의 Carl June, M.D.는 세포 치료 분야의 또 다른 선두 주자라고 설명했다.
개조 된 T 세포가 실험실에서 수백만 개로 "확장"된 후 환자에게 다시 주입됩니다. 모든 것이 계획대로 진행된다면, CAR T 세포는 환자의 몸에서 계속 증식 할 것이며, 조작 된 수용체의지도하에 표면에 표적 항원을 보유하고있는 암세포를 인식하고 죽일 것입니다.
현재까지 FDA에 의해 승인된 CAR T 세포 요법은 B 세포 상의 두 항원, CD19 또는 BCMA 중 하나를 표적으로 한다.
CAR T 셀 만들기
점점 더 많은 수의 CAR T-세포 치료법이 임상 연구에서 개발되고 테스트되고 있습니다. 환자에서 어떻게 기능하는지에 영향을 줄 수있는 각 특정 치료법 간에는 중요한 차이점이 있지만 모두 유사한 구성 요소를 공유합니다. 각 CAR은 세포막을 연결합니다. 수용체의 일부는 세포 외부에 위치하며 일부는 세포 내에 위치한다. 세포 표면으로부터 밖으로 뻗어나가는 CAR의 부분은 일반적으로 실험실에서 만든 항체의 단편 또는 도메인으로 구성된다. 어떤 도메인이 사용되는지는 수용체가 종양 세포 상의 항원을 얼마나 잘 인식하거나 결합하는지에 영향을 미친다. 각 CAR의 내부 부분은 신호전달 및 "공동자극" 도메인을 갖는다. 이들은 수용체가 항원과 상호 작용 한 후에 세포 내로 신호를 전송합니다. 사용되는 다른 도메인은 세포의 전반적인 기능에 영향을 줄 수 있습니다.
거의 존재하지 않는 새로운 치료 옵션
CAR T 세포 요법의 초기 개발은 주로 소아에서 가장 흔한 암, 급성 림프모구성 백혈병 (ALL)에 초점을 맞추었다.
소아 ALL의 우세한 유형 인 B 세포에서 발생하는 ALL로 진단 된 어린이의 80 % 이상이 집중적 인 화학 요법으로 완치 될 것입니다. 그러나 효과적인 치료법은 화학 요법이나 줄기 세포 이식 후 암이 재발하거나 재발하는 환자에게는 제한적이었습니다.
그러나 2017 년에는 FDA가 재발 한 ALL을 가진 어린이의 암을 근절 할 수 있음을 입증하는 임상 시험을 기반으로 기관에서 승인 한 최초의 CAR T 세포 치료법 인 tisagenlecleucel (Kymriah)에 대한 FDA의 승인과 함께 새로운 옵션이 나타났습니다.
어떤 경우에는 CAR T-세포 요법이 충분히 오랫동안 연구되어 어린이의 장기적인 결과에 대한 세부 사항이 나타나기 시작했습니다.
예를 들어, NCI가 이끄는 연구팀은 최근 임상 시험의 일환으로 CAR T 세포로 치료 된 재발 된 ALL을 가진 어린이의 장기 추적 관찰에 대해보고했습니다. 어린이 절반 이상이 잠재적으로 치유 가능한 줄기 세포 이식을 받았으며 그 어린이의 약 60 %는 암이 재발하거나 질병 관련 문제를 경험하지 않고 5 년 후에도 여전히 살아 있음을 발견했습니다.
ALL을 앓고있는 어린이의 CAR T 세포 요법으로 이루어진 진전은 "환상적이었습니다."라고 NCI와 최근에는 콜로라도 아동 병원에서 CAR-T 세포 요법의 여러 임상 시험을 주도 한 테리 프라이 (Terry Fry) 박사는 말했다. 프라이 박사는 CAR T-세포 요법이 더 널리 보급됨에 따라 재발 된 ALL을 가진 어린이를위한 보살핌의 표준이되었다고 말했다.
CD19 표적 CAR T 세포는 또한 진행된 공격적인 림프종을 가진 성인과 어린이에게 희망을 제공하고 있다. CAR T 세포가 개발되기 전에,이 환자들 중 많은 사람들이 "사실상 치료할 수 없었다"고 NCI의 암 연구 센터 (Center for Cancer Research)의 제임스 코첸더퍼 (James Kochenderfer) 박사는 확산성 거대 B 세포 림프종 환자에서 CAR T 세포 치료법에 대한 여러 시험을 이끌었다고 말했다.
Kochenderfer 박사는 현재까지 림프종의 결과는 "믿을 수 없을만큼 성공적이었다"며 "CAR T 세포는 여러 유형의 림프종에 자주 사용되는 치료법이되었습니다."
CAR T-세포 요법의 부작용 이해 및 관리
모든 암 치료와 마찬가지로, CAR T 세포 요법은 항체 생성 B 세포의 대량 사멸 및 감염을 포함하여 심각한 부작용을 일으킬 수 있다. 가장 빈번하고 심각한 부작용 중 하나는 사이토 카인 방출 증후군 (CRS)입니다.
면역 관련 의무의 일환으로, T 세포는 면역 반응을 자극하고 지시하는 데 도움이되는 사이토 카인 화학 메신저를 방출합니다. CRS의 경우, 주입 된 T 세포는 혈류에 사이토 카인을 범람시켜 위험한 고열과 혈압의 급한 강하를 포함하여 심각한 부작용을 일으 킵니다. 어떤 경우에는 심각한 CRS가 치명적일 수 있습니다.
역설적이게도, CRS는 CAR T-세포 요법의 "표적에" 효과로 간주된다 - 즉, 그것의 존재는 T 세포가 체내에서 작용하고 있음을 증명한다. 일반적으로 신체에서 가장 광범위한 양의 암을 앓고있는 환자는 CAR T 세포에서 심각한 CRS를 경험할 가능성이 더 높다고 Kochenderfer 박사는 설명했다.
많은 환자에서, 어린이와 성인 모두에서, 경미한 형태의 CRS는 스테로이드를 포함한 표준 지원 요법으로 관리 될 수 있습니다. 그리고 연구자들은 CAR T-세포 치료에 대한 더 많은 경험을 쌓았을 때, CRS의 더 심각한 사례를보다 잘 관리 할 수있는 방법을 발견했습니다.
그 관리의 큰 부분은 약물 tocilizumab (Actemra)입니다. 처음에는 청소년 관절염과 같은 염증성 상태를 치료하는 데 사용된이 약물은 T 세포 및 대식세포에 의해 대량으로 종종 분비되는 사이토 카인 인 IL-6의 활성을 차단합니다.
CAR T-세포 요법과 관련된 특별한 우려의 다른 부작용은 심각한 혼란, 발작-유사 활성, 및 언어 장애를 포함하는 신경학적 효과이다. 이러한 신경 학적 부작용 (면역 이펙터 세포 관련 신경 독성 증후군 또는 ICANS라고도 함)의 정확한 원인은 아직 명확하지 않습니다.
CRS 치료에 효과적이지만 tocilizumab은 ICANS에 도움이되지 않는 것 같습니다. 스테로이드는 현재 중증 ICANS, 특히 덱사메타손을위한 최상의 치료 옵션이며, 다른 스테로이드보다 중추 신경계를 관통하는 것이 더 낫다고 NCI의 암 연구 센터에서 CAR T 세포 치료법의 여러 시험에 관여하는 Jennifer Brudno, M.D.는 설명했다.
CRS와 ICANS를 예방하는 다양한 방법이 현재 집중적 인 연구 중이라고 Brudno 박사는 말합니다. 한 가지 접근법은 토실리주맙과 저용량 스테로이드의 예방적 사용이다. 더 많은 연구가 필요하지만 "지금까지의 데이터는 안심할 수 있다"고 그녀는 말했다.
ICANS에 대한 다른 치료법이 조사되고 있습니다. 예를 들어, 소규모 연구에 따르면 류마티스 관절염 치료에 사용되는 아나킨라 (Kineret)가 CAR T 세포 요법으로 치료받는 환자의 심각한 ICANS를 예방하는 데 도움이 될 수 있음을 발견했습니다.면책 조항 종료.
심각한 CRS와 ICANS로부터 보호하기위한 또 다른 아이디어는 CAR 자체를 수정하는 것이라고 Brudno 박사는 설명했습니다.
예를 들어, 림프종을 가진 성인의 작은 임상 시험에서, NCI에서 개발 된 "리모델링 된"CD-19 표적 CAR T 세포로 치료 된 환자는 동일한 CAR의 원래 형태로 역사적으로 볼 수있는 것보다 훨씬 적은 심각한 신경 학적 부작용을 보였다.
고형 종양을 포함하는 더 많은 표적 항원
CAR T 세포에 대한 연구는 수백 건의 진행 중인 임상 시험을 포함하여 빠른 속도로 계속되고 있습니다. 이 확장의 일부는 CAR T 세포에 대한 좋은 표적이 될 수있는 종양 세포에 대한 추가 항원을 확인한 연구자의 산물입니다.
CD19와 BCMA가 FDA가 승인한 CAR T-세포 요법이 있는 유일한 항원이지만, 한 번에 여러 항원을 표적으로 하는 치료법을 포함하여 혈액암에서 흔히 발견되는 다른 항원을 표적으로 하는 CAR T-세포 치료법이 개발되었다.면책 조항 종료.
그러나 CAR T 세포를 사용하여 뇌, 유방 또는 신장암과 같은 고형 종양을 치료하는 것은 어떻습니까? 거기에서, 진보는 얻기가 어려웠습니다. 고형 종양의 표면에 있지만 건강한 세포가 아닌 항원을 확인하려는 노력은 "크게 성공하지 못했다"고 Rosenberg 박사는 말했다.
고형 종양의 또 다른 장애물은 주변 환경입니다. 물리적 장벽은, 예를 들어, 주입된 CAR T 세포가 종양 세포에 도달하는 것을 방지할 수 있다. 종양 세포 또는 다른 면역 세포에 의해 생성 된 면역 억제 분자와 같은 미세 환경의 다른 구성 요소는 CAR T 세포가 오작동을 일으켜 세포 살상 의무를 수행 할 수 없게 할 수 있습니다.
아마도 가장 큰 장벽은 "오래된 문제 : 종양 이질성"이라고 스탠포드 대학의 Parker 암 면역 요법 연구소 소장 인 Crystal Mackall, M.D.는 말했다.
즉, 동일한 암 유형의 고형 종양은 환자마다 그리고 심지어 특정 환자 내에서도 분자적으로 상당히 다를 수 있습니다. 예를 들어, 일부 종양 세포에는 표적이 가능한 항원이 없거나 CAR T 세포가 예상대로 기능하기에 충분하지 않을 수 있습니다.
Despite these obstacles, researchers continue to try to find ways to use CAR T cells to treat solid tumors.
One approach involves trying to outwit the immune-suppressing environment of many advanced solid tumors. Several research groups, for example, have developed what are known as “armored” CAR T cellsExit Disclaimer that can navigate through this difficult microenvironment by secreting specific cytokines and other molecules.
Other researchers are pursuing more conventional approaches, relying on standard CAR-engineering technologies and targeting a single surface antigen on cancer cells.
예를 들어, 실험실 및 동물 기반 연구에서 유망한 결과를 얻은 후, 스탠포드의 Mackall 박사 그룹은 B7-H3라고 불리는 고형 종양에서 단백질을 표적으로 삼는 CAR T 세포 요법에 대한 NCI가 지원하는 임상 시험을 시작했습니다. 또 다른 시험에서, 그녀의 그룹은 DIPG라고 불리는 균일하게 치명적인 뇌암을 앓고있는 일부 어린이와 젊은 성인에서 GD2라고 불리는 암세포에 분자를 표적으로 삼는 CAR T 세포 요법을 조사하고 있습니다.
GD2 CAR T-cell 임상시험의 경우, 처음에 어떻게 구상되었는지, 어떻게 수행되었는지는 상당히 다르다고 맥칼 박사는 2021년 암 면역요법 학회 연례 회의에서 설명했다.
초기에, 환자들은 CAR T 세포의 초기 정맥내 주입으로만 치료될 예정이었다. 그러나 유사한 CAR T 세포 요법에 대한 동물 모델 연구 결과는 연구자들이 시험을 변경하도록 이끌었다 : 초기 정맥 내 주입에 반응하는 환자는 뇌에 직접 주입 된 추가 더 작은 용량을 받았다.
그녀는 환자에게 여러 번 투여 할 수있는 능력은 종양 반응 (예 : 종양 크기의 감소)과 암 관련 증상의 개선을 가져 왔다고보고했다.면책 조항 종료.
연구팀은 또한 임상시험에 사용된 GD2 CAR T 세포와 그 제조 방법을 신속하게 변형하여 잠재적인 효능과 안전성을 향상시킬 수 있었습니다. 이러한 신속한 변화를 일으킬 수있는 능력은 세포 요법을 통한 지속적인 혁신의 중요성을 강조한다고 맥콜 박사는 말했다.
"이 분야의 우리 모두는 우리가 이러한 CAR T 세포 엔지니어링과 관련하여 우리가 할 수있는 일에 대해 빙산의 일각을 긁고 있다는 것을 알고 있다고 생각합니다."라고 그녀는 말했습니다. "고형 종양에서 [효과]를 제한하는 문제에 대한 많은 차세대 접근법이 있습니다."
기성품 CAR T 세포 요법: CRISPR, 자연 살해자 및 mRNA
연구자들은 또한 CAR T 세포 요법을위한 면역 세포의 원천을 재고하기 시작했습니다 - 환자가 아니라 건강한 기증자로부터 수집 된 T 세포를 사용합니다. 목표: "기성품" CAR T-세포 요법은 각 환자에 대해 제조될 필요 없이 즉시 사용할 수 있습니다.
FDA가 승인한 모든 CAR T-세포 치료제는 CAR을 생산하기 위해 유전 물질을 T 세포로 전달하기 위해 무장 해제된 바이러스에 의존합니다. 그러나 현재 소규모 임상 시험에서 테스트되고 있는 기성품 CAR T 세포의 경우, TALON 및 CRISPR과 같은 유전자 편집 기술이 기증된 T 세포가 CAR을 생산하도록 유도하는 데 사용되고 있습니다.
다른 기성품 CAR은 또한 자연 살해 (NK) 세포라고 불리는 다른 유형의 면역 세포를 사용합니다. 이 연구의 대부분은 아직 초기 단계에 있지만 일부 CAR NK 세포 치료법은 이미 소규모 임상 시험에서 테스트되고 있습니다.
그리고 T 세포의 근원과 면역 세포의 유형이 재고려되고 있을뿐만 아니라 치료법이 실제로 만들어지는 곳도 마찬가지입니다. 예를 들어, 몇몇 연구 그룹은 CAR T 세포가 신체 내에서 생성 될 수 있도록 나노 기술 및 mRNA 기반 접근법을 사용하고 있습니다.
마지막 도랑 암 치료법이 아닌가?
대부분의 경우, CAR T 세포 치료는 여러 가지 다른 치료 후에 사람의 암이 이미 악화 될 때까지 고려 사항이 아닙니다. 그러나 그것은 변화하기 시작했습니다.
최근에, 두 번의 대규모 임상 시험에서, CAR T-세포 요법은 비호지킨 림프종 환자들에 대한 표준 치료보다 더 효과적임이 입증되었으며, 그의 암은 그들의 초기 또는 첫 번째 라인, 화학요법 후에 재발하였다.
이 발견으로 인해 일부 전문가들은 이러한 환자들에게 CAR T 세포 요법이 곧 표준 두 번째 라인 치료로 더 많은 화학 요법을 대체 할 수 있다고 결론 지었다.
프라이 박사는 ALL을 가진 일부 어린이의 경우, 이런 식으로 CAR T 세포를 사용하는 것이 특히 매력적이라고 말했다. 특히, 그는 초기 화학 요법 후 재발 위험이 높은 아이들을 지적했는데, 이는 일반적으로 약 2.5 년 동안 투여됩니다. 실제로 초기 화학 요법 치료에 최적의 반응을하지 않는 ALL을 가진 어린이의 CAR T 세포에 대한 소규모 임상 시험이 이미 진행 중입니다.
잘 반응하는 환자의 경우 "2 년 더 화학 요법을 절약 할 수 있습니다."라고 Fry 박사는 말합니다. "생각해보면 놀랍습니다."
단순한 CAR T 세포 이상: TILs 및 TCR
CAR T 세포는 세포 요법과 관련하여 사자의 관심을 끌었습니다. 그러나 다른 유형의 세포 치료법도 고형 종양 환자를 포함한 소규모 임상 시험에서 약속을 보여주었습니다.
종양 침윤 림프구 (TILs)로 알려진 한 가지 유형은 종양 안팎의 환경에 침투 한 면역 세포를 사용합니다. NCI의 연구원들은 TIL을 사용하여 진행성 암 환자를 성공적으로 치료한 최초의 연구자로, 처음에는 흑색종에서, 나중에는 자궁경부암을 포함한 여러 다른 암에서 치료했습니다. 최근 NCI 연구자들은 암에 특이적인 돌연변이를 가진 암세포를 인식하는 TIL을 확인하는 기술을 개발했습니다.면책 조항 종료 암이 TIL 요법에 반응 할 가능성이 더 높은 사람들을 식별합니다.
다른 유형의 세포 요법은 환자의 T 세포가 특정 T 세포 수용체 (TCR)를 발현하도록 엔지니어링하는 것을 포함합니다. 세포 표면에서만 특정 항원을 인식 할 수있는 합성 항체의 일부를 사용하는 CAR과 달리 TCR은 종양 세포 내부에있는 항원을 인식 할 수있는 자연 발생 수용체를 사용합니다.
현재까지 TCR T 세포는 다양한 고형 종양 환자에서 테스트되어 흑색종과 육종에서 약속을 보여줍니다.
- 업데이트 : 행진 10, 2022
이 콘텐츠의 일부 또는 전부를 재현하려면 저작권 및 권한에 대한 지침은 NCI 정보 재사용을 참조하십시오. 허용되는 디지털 복제의 경우, 국립 암 연구소를 출처로 인정하고 원래 제품의 제목을 사용하여 원래 NCI 제품에 링크하십시오. 예를 들어, "CAR T 세포 : 환자의 면역 세포를 치료하기위한 공학 그들의 암은 원래 국립 암 연구소 (National Cancer Institute)에 의해 출판되었습니다."
- 구글 번역으로 작성된 글로 문맥상 매끄럽지 않을 수 있습니다
'관심주' 카테고리의 다른 글
| 8월 31일 특징 종목 (0) | 2022.08.31 |
|---|---|
| 8월 31일 마감 시황 (0) | 2022.08.31 |
| 8월 30일 상한가 및 급등 종목 (2) | 2022.08.30 |
| 8월 30일 특징 종목 (2) | 2022.08.30 |
| 8월 30일 마감 시황 (2) | 2022.08.30 |






댓글